A Importância do pH para as Enzimas: Dê Um Exemplo Prático Da Importância Do Ph Das Enzimas
Dê Um Exemplo Prático Da Importância Do Ph Das Enzimas – As enzimas, moléculas proteicas essenciais para a vida, atuam como catalisadores biológicos, acelerando reações químicas em nossos organismos e em diversos processos industriais. Sua estrutura tridimensional intrincada é crucial para sua função. A conformação espacial precisa, determinada pela sequência de aminoácidos e pelas ligações entre eles (pontes de hidrogênio, interações hidrofóbicas, pontes dissulfeto), cria um sítio ativo específico onde os substratos se ligam e a reação ocorre.
Alterações nesse delicado arranjo, inclusive pela variação de pH, podem comprometer irreversivelmente a atividade enzimática.
A Influência do pH na Estrutura Enzimática
O pH do meio influencia diretamente as cargas elétricas dos aminoácidos que compõem a enzima. Aminoácidos com grupos ionizáveis, como ácido aspártico, ácido glutâmico, lisina e arginina, alteram suas cargas dependendo do pH. Em um pH muito ácido ou muito básico, essas mudanças de carga podem levar a alterações conformacionais na estrutura terciária e quaternária da enzima, afetando a disposição espacial do sítio ativo e, consequentemente, sua capacidade catalítica.
Em casos extremos, a enzima pode até sofrer desnaturação, perdendo completamente sua atividade.
Ação da Pepsina no Estômago, Dê Um Exemplo Prático Da Importância Do Ph Das Enzimas
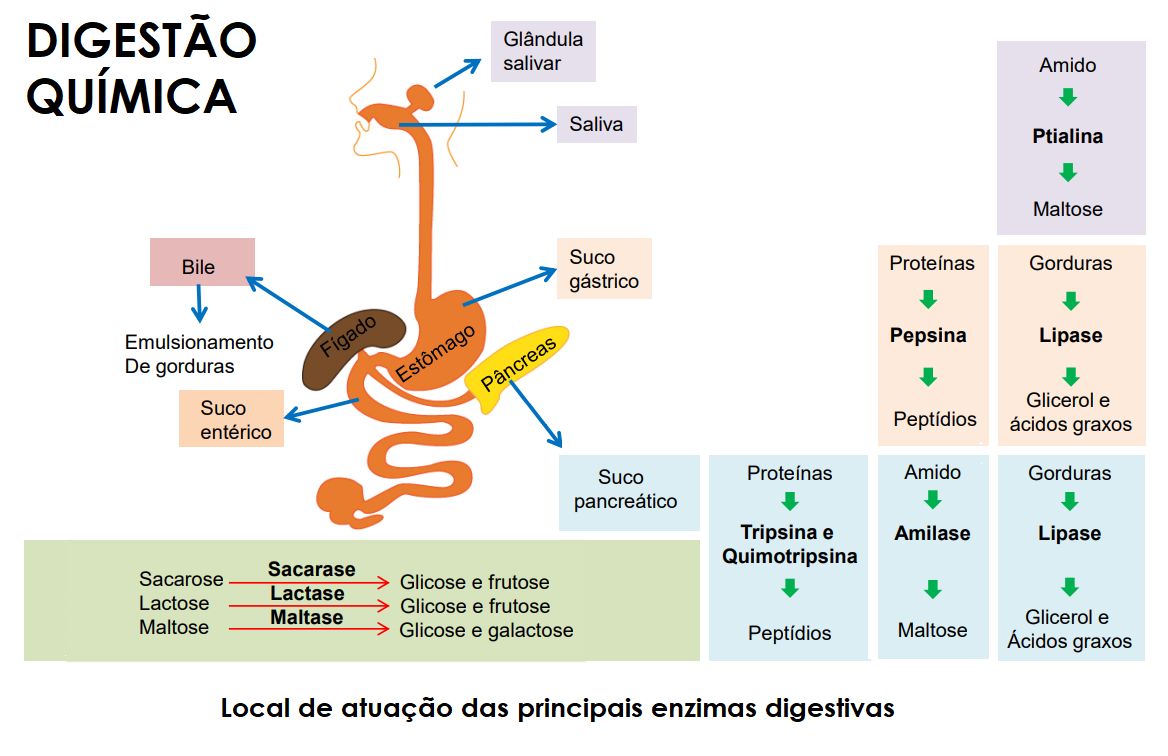
A pepsina, uma enzima digestiva, ilustra perfeitamente a importância do pH ótimo para a atividade enzimática. O estômago apresenta um ambiente extremamente ácido (pH entre 1,5 e 2,5), ideal para a ação da pepsina, que inicia a digestão de proteínas. Em pHs mais altos, a pepsina perde sua conformação ideal, diminuindo drasticamente sua eficácia.
| pH | Atividade Enzimática | Estrutura da Enzima | Observações |
|---|---|---|---|
| 1,5 | Alta | Conformação ótima | Sítio ativo acessível e funcional. |
| 3,0 | Moderada | Algumas alterações conformacionais | Redução na eficiência catalítica. |
| 5,0 | Baixa | Alterações significativas na estrutura | Sítio ativo parcialmente inacessível. |
| 7,0 | Mínima/Nula | Desnaturação parcial ou completa | Perda da função catalítica. |
Ação da Tripsina no Intestino Delgado

Em contraste com a pepsina, a tripsina, outra enzima digestiva, atua no intestino delgado, um ambiente alcalino (pH entre 7,5 e 8,5). Seu pH ótimo reflete a necessidade de um ambiente específico para manter sua estrutura tridimensional e garantir a eficácia na digestão de proteínas.
- Em pH 7,5 – 8,5: A tripsina apresenta atividade máxima, quebrando eficientemente as ligações peptídicas.
- Em pH 7,0: A atividade enzimática diminui, devido a alterações conformacionais iniciais.
- Em pH 6,0: A atividade é significativamente reduzida, com perda considerável da eficiência.
- Em pH 9,0: Observa-se uma redução na atividade, embora menos drástica que em pHs mais baixos. Isso demonstra que a faixa ótima possui uma certa flexibilidade, porém com limites.
- Em pHs extremos (acima de 10 ou abaixo de 5): A tripsina sofre desnaturação, perdendo completamente sua atividade.
A eficácia da tripsina na digestão proteica depende diretamente da manutenção de seu pH ótimo. Desvios significativos podem levar à inativação da enzima e comprometimento do processo digestivo.
Enzimas em Detergentes
Muitos detergentes contêm enzimas, como proteases e amilases, para auxiliar na remoção de manchas de proteínas e amido, respectivamente. A formulação do detergente leva em consideração o pH ótimo dessas enzimas. Geralmente, o pH é ajustado para garantir a máxima atividade enzimática na temperatura de lavagem.
- Vantagens: Remoção mais eficiente de manchas, menor necessidade de água quente, redução do impacto ambiental.
- Desvantagens: Algumas enzimas podem ser inativadas em pHs muito altos ou baixos ou em temperaturas extremas; possível irritação da pele em indivíduos sensíveis.
A otimização do pH é crucial para garantir a eficácia das enzimas nos detergentes, maximizando sua capacidade de limpeza e minimizando os impactos negativos.
Representação Gráfica da Atividade Enzimática em Diferentes pHs
Um gráfico da atividade enzimática em função do pH tipicamente apresenta uma curva em formato de sino. O ponto mais alto da curva representa o pH ótimo, onde a atividade enzimática é máxima. À medida que o pH se afasta do ótimo, a atividade enzimática diminui, aproximando-se de zero em pHs extremos. A inclinação das laterais da curva indica a sensibilidade da enzima à variação de pH.
Uma curva mais estreita indica maior sensibilidade, enquanto uma curva mais ampla indica maior tolerância a variações de pH.
A análise deste gráfico é fundamental para determinar o pH ótimo de uma enzima e compreender sua sensibilidade às variações de pH, informações cruciais para aplicações biotecnológicas e biomédicas.
Em resumo, a influência do pH na atividade enzimática é um pilar fundamental da bioquímica e de diversas aplicações tecnológicas. Compreender como variações mínimas de pH podem afetar a estrutura e a função dessas proteínas essenciais nos permite otimizar processos, desenvolver novas tecnologias e, principalmente, desvendar os segredos da complexa maquinaria da vida. Da digestão humana à produção de detergentes, a otimização do pH para garantir a eficácia enzimática é crucial.
A observação de como a pepsina e a tripsina atuam em seus respectivos ambientes ideais ilustra perfeitamente a estreita relação entre pH e atividade catalítica. A busca pela compreensão dessa interação continua, abrindo caminho para avanços significativos em diversas áreas do conhecimento.

